第9回日本心臓財団メディアワークショップ「睡眠時無呼吸症候群(SAS)」
あらゆる心疾患の終末像である心不全とSASには深い関係がある。百村伸一氏は、心不全の概要について説明した後、SASが心不全を引き起こすメカニズムや、逆にSASが心不全から受ける影響を解説。SASと合併した心不全の治療については、「SASが閉塞型か中枢型かを判別したうえで、CPAPをはじめとした機器を用いて治療することが大切だ」と強調した。
日本では心不全の死亡率が増加中
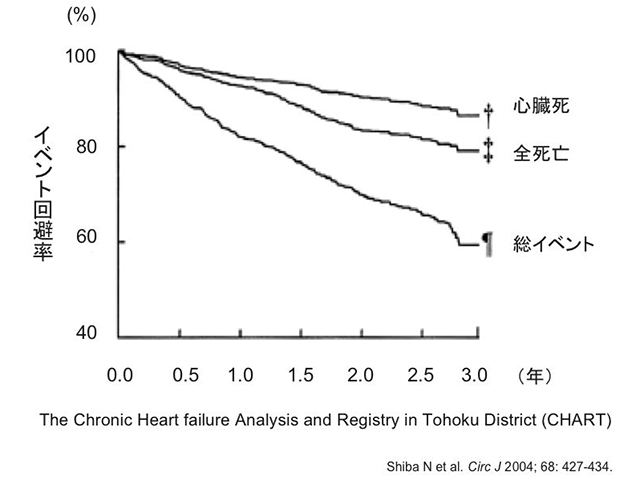 図2.増加し続ける心不全による死亡
図2.増加し続ける心不全による死亡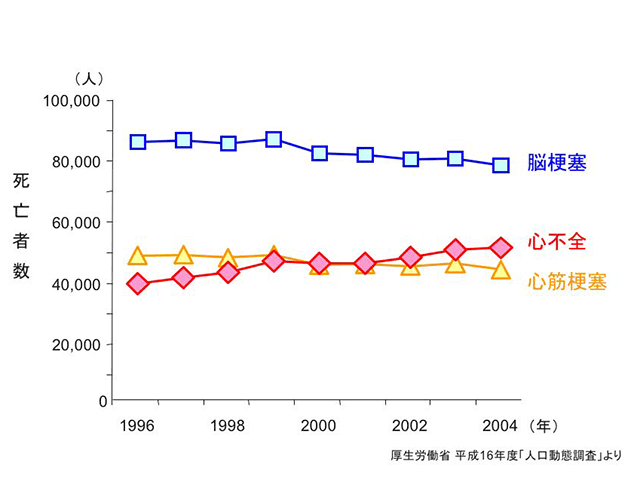
米国心臓病学会(ACC)と米国心臓協会(AHA)が合同で発表した慢性心不全治療ガイドラインによると、「心不全とは、心室を充満あるいは駆出する能力を損なうような、あらゆる構造上または機能上の心臓障害に起因する症候群である」と定義されている。言い換えれば、全身に必要な血液を送り出すポンプとしての心臓の機能に障害が起こっている状態である。これは、弁膜症・心筋症・心筋梗塞などを発症した後に適切な治療がなされずに心機能が落ちた際に現れる、あらゆる心疾患の終末像である。
心不全患者は、労作時の息切れやむくみなどの症状が現れるとともに、予後にも悪影響が及び、死亡率も高まる。わが国で心不全患者を対象に予後を追跡した疫学研究CHART(The Chronic Heart Failure Analysis and Registry in Tohoku District)によると、心不全患者の死亡率は3年間の追跡期間で約20%、1年間でも約7%となっている(図1)。また、わが国では近年、脳梗塞や心筋梗塞による死亡は減少しているものの、それに取って代わるかのように心不全による死亡の増加が認められる(図2)。この原因として、高齢化のほかに、心筋梗塞をはじめとした急性心疾患患者に対する救命率の向上により、急性期に心臓に受けたダメージの影響から慢性期に心不全に移行して死亡する症例が増加していることが考えられる。
閉塞型無呼吸は心不全の発症に関与し、中枢型無呼吸は心不全の悪化に関与する
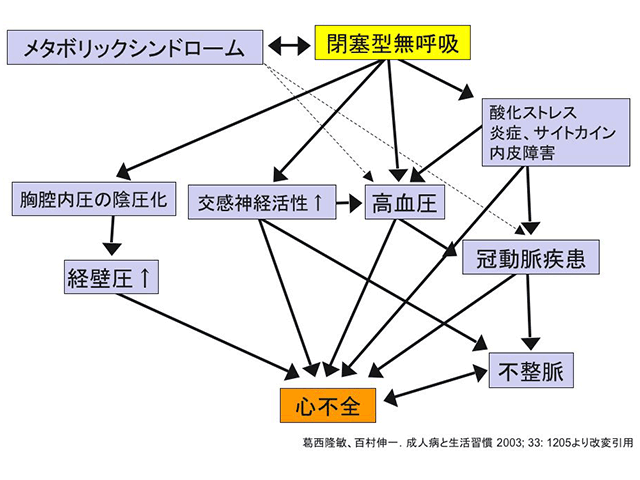 図4.慢性心不全から中枢型無呼吸に至る機序
図4.慢性心不全から中枢型無呼吸に至る機序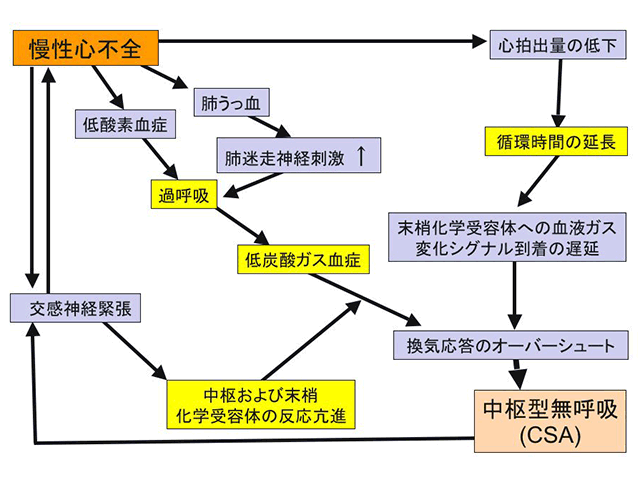
睡眠時無呼吸症候群(SAS)は心不全の発症・進展の過程で、重要な役割を果たしている。なかでも、気道閉塞によって起こる閉塞型睡眠時無呼吸(OSA)は、心不全の発症に強く関与している。一方、呼吸中枢の障害で起こる中枢型睡眠時無呼吸(CSA)は、心不全の結果として起こる無呼吸であり、さらに心不全を進展・悪化させると考えられている。海外では、心不全患者の約7割がこれらのうちいずれかを合併しているという報告も示されている。
OSAは交感神経の緊張を高めるとともに血圧も上昇させるほか、炎症性の細胞障害を引き起こすサイトカインの増加や、胸腔内圧の陰圧化などを引き起こす(図3)。とくに胸腔内圧の陰性化は、心臓の収縮の際に心臓壁に大きな負荷をもたらす。これらの積み重ねが心機能を低下させ、心不全の発症に至ることとなる。
心不全によって起こるCSAは、心不全の慢性化により肺の静脈圧上昇をもたらし、肺うっ血を引き起こす(図4)。その結果、肺迷走神経刺激が亢進し、過呼吸に陥る。これにより、血液中の炭酸ガス濃度が低下し、中枢および末梢の化学受容体がこれを感知して、呼吸を抑制しようとする。また、心不全は交感神経の緊張を招くが、これが化学受容体の反射を亢進するために呼吸の抑制が過剰になる。こうして起こった無呼吸がさらに交感神経の緊張を高め、心不全を悪化させるという悪循環に陥ってしまう。加えて、慢性心不全では心拍出量が低下するため血液の体循環の時間が長くなるが、これによって末梢化学受容体への信号伝達が遅れてしまうことも、呼吸の調節がうまくいかない一因と考えられる。こうした一連のメカニズムが、CSAが心不全を進展・増悪させる。
OSA合併心不全にはCPAP療法が有効
心不全患者のなかでも、無呼吸の回数が多い群は、回数が少ない群よりも死亡率が高くなることが海外の研究から明らかになっている。したがって、SASを合併した心不全患者は、一般的な心不全治療と平行してSASの治療を行うことで、心不全の予後がより改善されると考えられる。
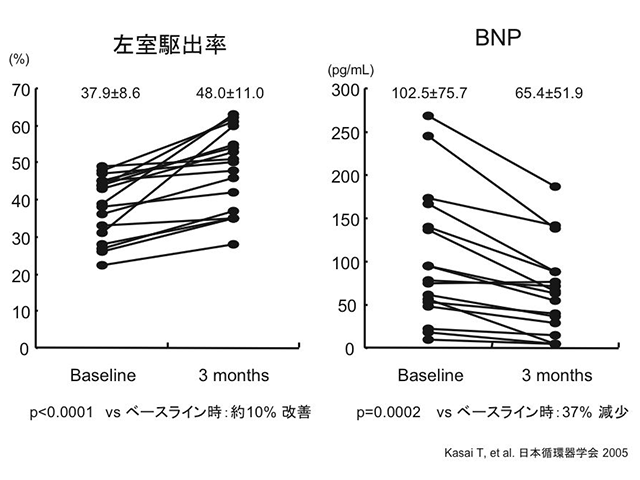
OSAに対する治療としては、CPAP療法の施行が推奨される。左室機能が低下した重症心不全患者にCPAP療法を行った研究によると、3カ月間で心臓のポンプ機能の指標とされる左室駆出率が10%改善し、心不全の重症度を測る指標とされる脳性ナトリウム利尿ペプチド(BNP)の血中濃度が37%減少したと報告されている(図5)。これらの知見により、CPAP療法がOSAを合併する心不全の予後と心機能を改善することのコンセンサスが得られつつある。また、OSAの患者は肥満者が多い傾向があるため、生活習慣への介入も必要となる。一方で、肥満でなくとも顎の構造的問題のためにOSAを発症するケースも日本人には比較的多い。その場合は耳鼻科への受診も検討する。
CSAにはBi-level PAPやASVなどの新デバイスが効果あり
一方、CSAの治療についても、CPAPは治療の基本とされているが、海外では必ずしも全ての患者に効果を発揮しないことが報告されている。そこで、CPAPを改良して吸気と呼気をそれぞれ補助する二段階の陽圧を設定できるようにしたBi-level PAPという機器が注目されている。虎の門病院で行われた研究によると、Bi-level PAPを用いてCSAの患者を治療した結果、AHIが約80%減少するといった劇的な改善に加え、左室駆出率やBNPも有意に改善したというデータが示されている。さらに、新たな治療法として、適応補助換気(ASV)療法という、Bi-level PAPをさらに改良したデバイスを用いた治療も実現されており、今後の普及が期待される。
また、在宅酸素療法(HOT)は、現在わが国の慢性心不全治療ガイドラインで採用されているものの、無呼吸に対する効果はさほど期待できない。ただし、SASの専門家の協力が得られないケースや、陽圧マスクの装着に抵抗感をもつ患者に対しては、使用に値すると考えられる。
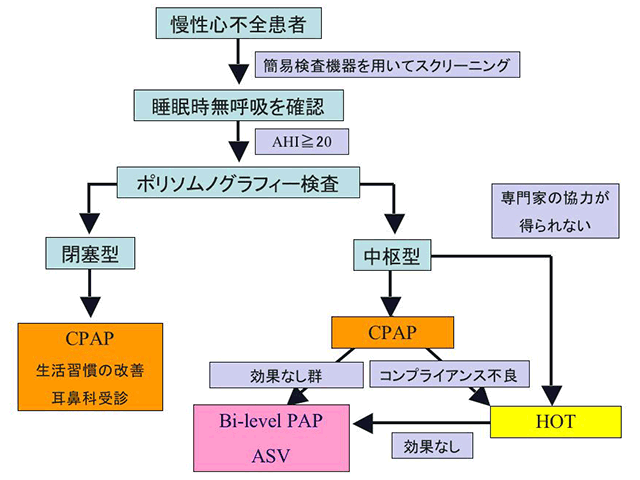
百村氏は講演の最後に、慢性心不全患者に対する現時点での治療戦略として図6を示し、「まずは簡易検査機器を用いてスクリーニングを行い、睡眠時の無呼吸がないか検査する必要がある。その結果、患者のAHIが20以上の場合には、さらに医療機関で一泊してポリソムノグラフィー検査を実施し、OSAとCSAを鑑別した後、それぞれに適した治療を行うことが重要だ」と訴えた。
INDEX
- 第25回 高血圧ゼロを目指す、循環器疾患予防の最新トレンド!―家庭と地域での取り組み―
- 第24回『心房細動』の診断・治療における最新トレンド―AIや家庭で取得したバイタルデータを活用した早期発見の可能性―
- 第23回 日常に潜む脳卒中の大きなリスク、『心房細動』対策のフロントライン―心不全の合併率も高い不整脈「心房細動」の最新知見―
- 第22回 高血圧パラドックスの解消に向けて―脳卒中や認知症、心不全パンデミックを防ぐために必要なこととは?―
- 第21回 健康を支える働き方改革「スローマンデー」の勧め―血圧と心拍数が教える健康的な仕事習慣―
- 第20回「家庭血圧の世界基準を生んだ「大迫(おおはさま)研究」30周年記念~家庭血圧普及のこれまでとこれから。最新知見とともに~
- 第19回「足元のひえにご注意! 気温感受性高血圧とは?」~気温と血圧、循環器病の関係~
- 第18回「2015年問題と2025年問題のために」~循環器疾患の予防による健康寿命の延伸~
- 第17回「ネット時代の健康管理」~生活習慣病の遠隔管理から被災地支援まで~
- 第16回「突然死や寝たきりを防ぐために…」~最新の動脈硬化性疾患予防ガイドラインから~
- 第15回「眠りとは?睡眠と循環器疾患」?こわいのは睡眠時無呼吸だけではない?
- 第14回日本心臓財団メディアワークショップ「コール&プッシュ!プッシュ!プッシュ!」?一般人による救命救急の今?
- 第13回日本心臓財団メディアワークショップ「心房細動治療はこう変わる!」
- 第12回日本心臓財団メディアワークショップ「新しい高血圧治療ガイドライン(JSH2009)」
- 第11回日本心臓財団メディアワークショップ「CKDと循環器疾患」
- 第10回日本心臓財団メディアワークショップ「特定健診・特定保健指導と循環器疾患」
- 第9回日本心臓財団メディアワークショップ「睡眠時無呼吸症候群(SAS)」
- 第8回日本心臓財団メディアワークショップ「動脈硬化を診る」
- 第7回日本心臓財団メディアワークショップ「新しい循環器医療機器の臨床導入をめぐる問題点」
- 第6回日本心臓財団メディアワークショップ「不整脈の薬物治療に未来はあるか」
- 第5回日本心臓財団メディアワークショップ「メタボリックシンドロームのリスク」
- 第4回日本心臓財団メディアワークショップ「高血圧診療のピットホール:家庭血圧に基づいた高血圧の管理」
- 第3回「突然死救命への市民参加:AEDは革命を起こすか」
- 第2回 「心筋梗塞は予知できるか」
- 第1回 「アブラと動脈硬化をEBMから検証する」